-
A
 Augusto Salazar Sandoval 3 years ago
Augusto Salazar Sandoval 3 years agoLes comparto otros cuatro ejercicios mas para que practiquen, los resolvemos en la sesión de hoy, todos, pero antes suban sus aportes.

-
A
 Augusto Salazar Sandoval 3 years ago
Augusto Salazar Sandoval 3 years agoUnos ejercicios para que se entretengan el fin de semana, ahora le subimos un poquito el nivel.
No se olviden de compartir sus aportes, también a lo propuesto por la profesora Rocio, y si tienen ejercicios adicionales subanlos y los resolvemos juntos.
Muchas gracias y buen fin de semana.

-
F
 Fatima Huamanchumo Soria 3 years ago
Fatima Huamanchumo Soria 3 years agoBuenas tardes profesor escribo para enviar la resolución de mis ejercicios aunque no se si estan bien.


-
A
 Augusto Salazar Sandoval 3 years ago
Augusto Salazar Sandoval 3 years agoAgradecerte Fatima, por tu compromiso con tus compañeros en resolver los ejercicios.
Chicos y chicas recuerden que el compromiso es uno de los pilares sobre los cuales se edifica el exito.
-
A
 Augusto Salazar Sandoval 3 years ago
Augusto Salazar Sandoval 3 years agoFelicitaciones por tus aportes, y esta muy bien tu razonamiento en el plantamiento de los ejerccios, pero te sugiero tengas en consideración lo siguiente:
Ejercicio Nº11: Resolución conforme.
Ejercicio Nº12:
1.- Es un proceso isometrico, porque el volumen es constante (recipiente rigido).
2.- No has considerado P2, en el ejercicio, así obtendras la respuesta.
3.- Revisa bien la operación en la que despejas, T2
Ejercicio Nº13:
1.- El volumen captado del gas (0.78 litros) a 20.1ºC es decir 293.1ºK, y no a 309.65ºK (36.5ºC), a esta temperatura se da la reaccion quimica de fermentación, por lo que el calculo del numero de moles no corresponde, en 2 sesiones veremos estequiometria ahi te explico con mayores detalles.
2.- Te comparto un dato interesante, si te das cuenta es un proceso isobárico, la presion es constante (1 ATM: poresion atmosferica), aplica las ecuaciones de este tipo, y obtendras el resultado.
Ejercicio Nº14:
1.- Recuerda que el oxigeno se encuentra en la naturaleza en forma molecular y no atómica, es decir, en la forma O2, eso hace que su masa molecular es distinta a la que calculaste (16 g/mol) y es 16*2 g/mol = 32 g/mol, considera esto y obtendras la respuesta al ejercicio.
Estamos atentos a tus planteamientos.
Jóvenes acompañen a Fatima en la solución de los ejercicios, en la diversidad encontraremos mejores soluciones.
-
F
 Fatima Huamanchumo Soria 3 years ago
Fatima Huamanchumo Soria 3 years agoBuenas noches profesor escribo para decirle que ya corregi los ejercicios.


-
Y
 Yameli Sophia Carpio Marcos 3 years ago
Yameli Sophia Carpio Marcos 3 years agoBuenas noches profesor, aquí adjunto mi resolución al problema 9.
Profesor, intentaré resolver el resto de problemas y subire mi resolución.
Gracias.

-
IIsabel Guzmán Montoya 3 years ago
Buenos días profesor, aquí le subo mis respuestas âºï¸


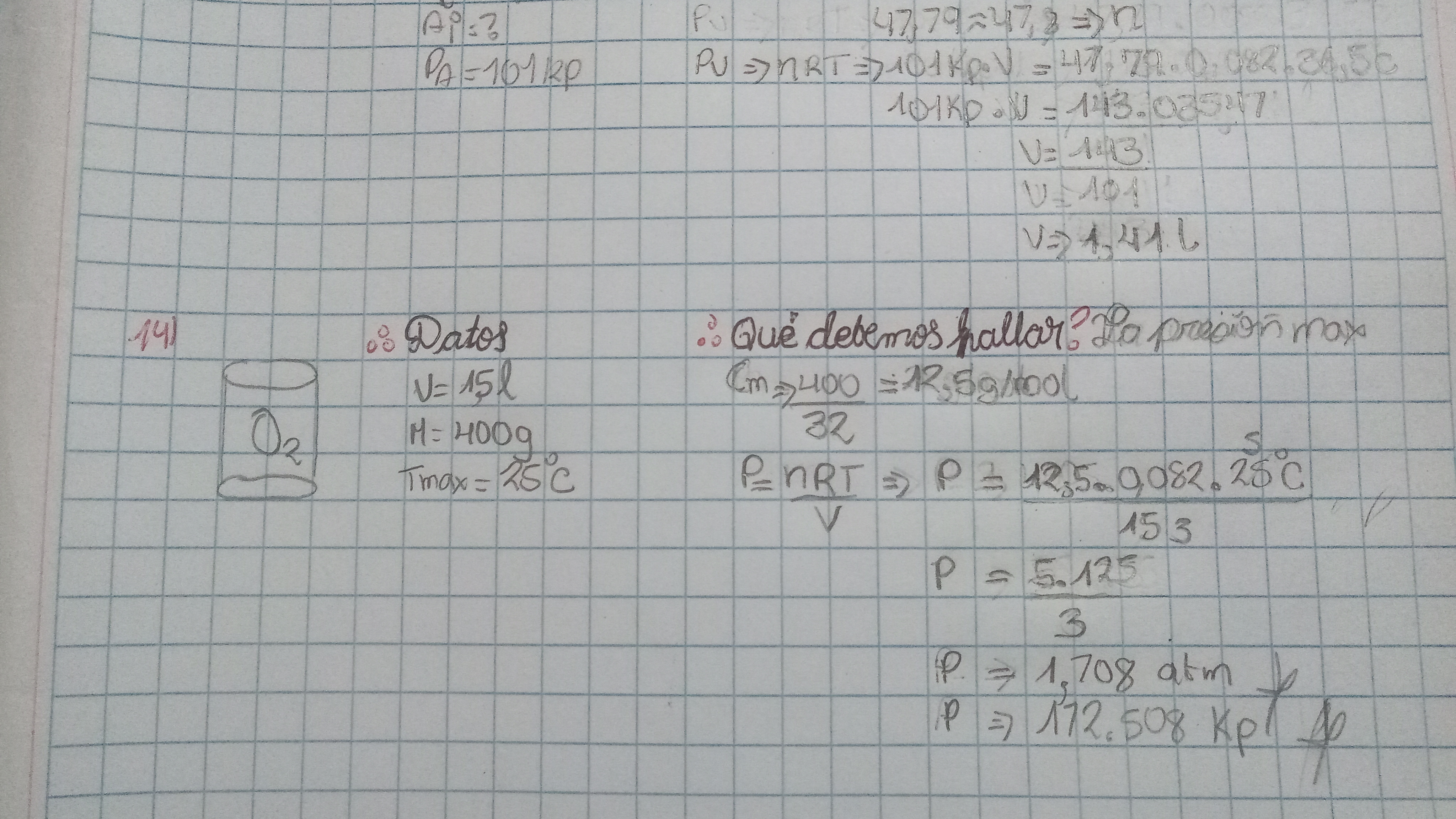
-
A
 Augusto Salazar Sandoval 3 years ago
Augusto Salazar Sandoval 3 years agoIsabel ten en consideración que debes trabajar con temperaturas absolutas es decir en grados Kelvin [ºK], decir convertir de [ºC] a [ºK]
-
IIsabel Guzmán Montoya 3 years ago
Buenos días profesor, aquí le subo mis respuestas ð




Por favor Inicia sesión o Regístrate para dejar una respuesta.